Geometria molecular é o estudo de como os átomos estão distribuídos espacialmente em uma molécula. Esta pode assumir várias formas geométricas, dependendo dos átomos que a compõem. As principais classificações são linear, angular, trigonal plana, piramidal e tetraédrica. É um parâmetro de importância fundamental para a previsão da polaridade de uma molécula.[1]
Para se determinar a geometria de uma molécula, é preciso conhecer a teoria da repulsão dos pares eletrônicos da camada de valência.
Índice
[esconder]Teoria da repulsão dos pares eletrônicos[editar | editar código-fonte]
A teoria da repulsão dos pares eletrônicos da camada de valência (TRPECV), proposta por R. Gillespie (1963), aponta que os pares eletrônicos (elétrons de valência, ligantes ou não) do átomo central se comportam como nuvens eletrônicas que se repelem e, portanto, tendem a manter a maior distância possível entre si. Mas, como as forças de repulsão eletrônica não são suficientes para que a ligação entre os átomos seja desfeita, essa distância é verificada no ângulo formado entre eles.
Tipos de geometria molecular[editar | editar código-fonte]
Existe a geometria angular; geometria piramidal trigonal; e a geometria tetraédrica, depois existem a geometria linear que é composta pela ligação covalente simples, ligação covalente dupla e ligação covalente tripla.
- Linear: Acontece em toda molécula biatômica (que possui dois átomos) ou em toda molécula em que o átomo central possui no máximo duas nuvens eletrônicas em sua camada de valência. Exemplo: Ácido clorídrico (HCl) e gás carbônico (CO2). Ângulo de 180°.
- Trigonal plana ou triangular: Acontece somente quando o átomo central tem três nuvens eletrônicas em sua camada de valência. Estas devem fazer ligações químicas, formando um ângulo de 120° entre os átomos ligados ao átomo central. Obs: caso duas das nuvens eletrônicas forem de ligações químicas e uma de elétrons não ligantes a geometria é angular, como descrita abaixo. O ângulo é de 120º
- Angular: Acontece quando o átomo central tem três ou quatro nuvens eletrônicas em sua camada de valência. No caso de três, duas devem estar fazendo ligações químicas e uma não, formando um ângulo de 120 graus entre os átomos ligantes. Quando há quatro nuvens, duas devem fazer ligações químicas e duas não, formando um ângulo de 104° 34' (104,45°) entre os átomos.
- Tetraédrica: Acontece quando há cinco nuvens eletrônicas na camada de valência do átomo central e todas fazem ligações químicas. O átomo central assume o centro de um tetraedro regular. Ângulo de 109º 28'
- Piramidal: Acontece quando há quatro nuvens eletrônicas na camada de valência do átomo central, sendo que três fazem ligações químicas e uma não. Os três átomos ligados ao átomo central não ficam no mesmo plano. O ângulo é de 107°.
- Bipirâmide Trigonal: Acontece quando há seis nuvens eletrônicas na camada de valência do átomo central, todas fazendo ligação química. O átomo central assume o centro de uma bipiramide trigonal, sólido formado pela união de dois tetraedros por uma face comum. Como exemplo cita-se a molécula PCl5. Os ângulos entre as ligações são 120 graus e 90 graus.
- Octaédrica: Acontece quando há sete nuvens eletrônicas na camada de valência do átomo central e todas fazem ligações químicas formando ângulos de 90 graus e 180 graus.
Tabela de geometria molecular[editar | editar código-fonte]
| Domínios eletrônicos ou Nuvens eletrônicas | D.E. ligantes | D.E. não ligantes | Geometria | Ângulo das ligações | Exemplo | Imagem |
|---|---|---|---|---|---|---|
| linear | ||||||
| trigonal | ||||||
| angular | ||||||
| tetraédrica | 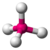 | |||||
| piramidal | ||||||
| angular | ||||||
| bipiramidal trigonal |  | |||||
| gangorra | ||||||
| forma de T | ||||||
| linear | ||||||
| octaédrica | 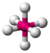 | |||||
| piramidal quadrada | ||||||
| quadrada plana | ||||||
| bipiramidal pentagonal | 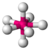 |
Ver também[editar | editar código-fonte]
Referências
- ↑ VALENTE, Mário; MOREIRA, Helena. (out/nov 2006). «Estrutura de Lewis e Geometria Molecular... mas não necessariamente por essa ordem!» (PDF). Sociedade Portuguesa de Química. Consultado em 20 jan 2013.
Nenhum comentário:
Postar um comentário