A entropia (do grego εντροπία, entropía), unidade [J/K] (joules por kelvin), é uma grandeza termodinâmica que mensura o grau de irreversibilidade de um sistema, encontrando-se geralmente associada ao que denomina-se por "desordem", não em senso comum [Nota 1] , de um sistema termodinâmico. Em acordo com a segunda lei da termodinâmica, trabalho pode ser completamente convertido em calor, e por tal em energia térmica, mas energia térmica não pode ser completamente convertida em trabalho. Com a entropia procura-se mensurar a parcela de energia que não pode mais ser transformada em trabalho em transformações termodinâmicas à dada temperatura.
A parcela de energia interna de um sistema em seu equilíbrio termodinâmico que não pode mais ser convertida em trabalho à temperatura de equilíbrio pode ser determinada pelo produto da entropia S pela temperatura absoluta T do sistema no respectivo estado, encontrando-se disponível à execução de trabalho por tal apenas a parcela 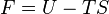 da energia interna U em consideração. A parcela de energia interna F que pode ser convertida em trabalho, assim como a entropia, é uma função de estadodo sistema, e por tal dá origem a um potencial termodinâmico: a energia livre de Helmholtz do sistema em consideração.
da energia interna U em consideração. A parcela de energia interna F que pode ser convertida em trabalho, assim como a entropia, é uma função de estadodo sistema, e por tal dá origem a um potencial termodinâmico: a energia livre de Helmholtz do sistema em consideração.
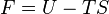 da energia interna U em consideração. A parcela de energia interna F que pode ser convertida em trabalho, assim como a entropia, é uma função de estadodo sistema, e por tal dá origem a um potencial termodinâmico: a energia livre de Helmholtz do sistema em consideração.
da energia interna U em consideração. A parcela de energia interna F que pode ser convertida em trabalho, assim como a entropia, é uma função de estadodo sistema, e por tal dá origem a um potencial termodinâmico: a energia livre de Helmholtz do sistema em consideração.
A entropia é uma grandeza que busca mensurar não a energia tampouco a matéria totais encerrada pelas fronteiras do sistema termodinâmico, mas sim como esta matéria e esta energia encontram-se armazenadas e distribuídas no sistema definido por tais fronteiras. Assim, embora uma grandeza bem distinta das grandezas massa, energia internae quantidade de matéria, a entropia de um sistema encontra-se certamente relacionada às grandezas citadas, sendo, da mesma forma que as anteriores, uma propriedade do sistema. A fim de definir-se um sistema simples especificam-se a energia interna U, a massa m - especificamente a quantidade de matéria N e a natureza das partículas que integram o sistema - e o seu volume V, e ao fazê-lo determina-se também, de forma automática, o valor da entropia S do sistema - uma grandeza escalar - no estado final a ser atingido uma vez dado tempo suficiente para que todos os processos necessários aconteçam. Assim a entropia S nos estados de equilíbrio termodinâmico é uma função das grandezas antes citadas:  .
.
 .
.
Ver-se-á que os processos que levam o sistema do estado inicial logo após ter sido isolado até o estado de final - o estado de equilíbrio termodinâmico - ocorrem sempre de forma a provocarem aumentos - ou no limite a manutenção - do valor da entropia do sistema. Não ocorrem processos que impliquem a diminuição da entropia total de umsistema isolado. A entropia é, pois, uma função de estado que obedece a um princípio de maximização, o "princípio da máxima entropia": a entropia em um estado de equilíbrio termodinâmico - satisfeitas as restrições impostas ao sistema - é sempre a máxima possível.
A entropia é uma função de estado cujo valor sempre cresce durante processos naturais em sistemas isolados; e quando escrita em função das grandezas extensivas energia interna U, volume V e número de elementos N - no caso dos sistemas termodinâmicos mais simples - a entropia  é, assim como as respectivas Transformadas de Legendre, uma equação fundamental para o sistema termodinâmico em questão. É, então, possível, a partir desta e de todo o formalismo termodinâmico, obter-se qualquer informação física relevante para o sistema em estudo. [Ref. 1] . Se expressa em função de uma ou mais grandezas que não as citadas - cônjugas a si - a expressão para a entropia S reduz-se a uma mera equação de estado. As equações de estado, embora relacionem valores de grandezas termodinâmicas nos estados de equilíbrio, não retêm em si, individualmente, todas as informações acerca do sistema. É necessário o conhecimento de todas as equações de estado para recuperar-se a completeza acerca das informações - para a partir delas se estabelecer uma equação fundamental - e via transformada de Legendre, se estabelecer qualquer das demais equações fundamentais - se desejada.
é, assim como as respectivas Transformadas de Legendre, uma equação fundamental para o sistema termodinâmico em questão. É, então, possível, a partir desta e de todo o formalismo termodinâmico, obter-se qualquer informação física relevante para o sistema em estudo. [Ref. 1] . Se expressa em função de uma ou mais grandezas que não as citadas - cônjugas a si - a expressão para a entropia S reduz-se a uma mera equação de estado. As equações de estado, embora relacionem valores de grandezas termodinâmicas nos estados de equilíbrio, não retêm em si, individualmente, todas as informações acerca do sistema. É necessário o conhecimento de todas as equações de estado para recuperar-se a completeza acerca das informações - para a partir delas se estabelecer uma equação fundamental - e via transformada de Legendre, se estabelecer qualquer das demais equações fundamentais - se desejada.
 é, assim como as respectivas Transformadas de Legendre, uma equação fundamental para o sistema termodinâmico em questão. É, então, possível, a partir desta e de todo o formalismo termodinâmico, obter-se qualquer informação física relevante para o sistema em estudo. [Ref. 1] . Se expressa em função de uma ou mais grandezas que não as citadas - cônjugas a si - a expressão para a entropia S reduz-se a uma mera equação de estado. As equações de estado, embora relacionem valores de grandezas termodinâmicas nos estados de equilíbrio, não retêm em si, individualmente, todas as informações acerca do sistema. É necessário o conhecimento de todas as equações de estado para recuperar-se a completeza acerca das informações - para a partir delas se estabelecer uma equação fundamental - e via transformada de Legendre, se estabelecer qualquer das demais equações fundamentais - se desejada.
é, assim como as respectivas Transformadas de Legendre, uma equação fundamental para o sistema termodinâmico em questão. É, então, possível, a partir desta e de todo o formalismo termodinâmico, obter-se qualquer informação física relevante para o sistema em estudo. [Ref. 1] . Se expressa em função de uma ou mais grandezas que não as citadas - cônjugas a si - a expressão para a entropia S reduz-se a uma mera equação de estado. As equações de estado, embora relacionem valores de grandezas termodinâmicas nos estados de equilíbrio, não retêm em si, individualmente, todas as informações acerca do sistema. É necessário o conhecimento de todas as equações de estado para recuperar-se a completeza acerca das informações - para a partir delas se estabelecer uma equação fundamental - e via transformada de Legendre, se estabelecer qualquer das demais equações fundamentais - se desejada.Índice
[esconder]Conceitos científicos de "desordem"[editar | editar código-fonte]
A associação incorreta da entropia com a "desordem" ao considerar-se o sentido em senso comum desta palavra leva muitas vezes a uma compreensão errônea da definição de entropia e também a usos completamente inadequados da segunda lei da termodinâmica [Nota 2] , e assim, vale estabelecer-se aqui pelo menos um conceito aceitável para o termo "desordem" que seja adequado ao meio científico.
Segundo a física estatística a desordem de um sistema pode ser associada - não diretamente mas mediante uma função logaritmo - ao número de microestados acessíveis ao sistema uma vez satisfeitas asrestrições impostas a ele. Restrições práticas comuns em sistemas termodinâmicos ligam-se geralmente ao valor da energia interna U e ao volume V disponíveis ao sistema, e aumentar a desordem de um sistema significa aumentar o número de microestados (de configurações) acessíveis às partículas deste sistema.
Um exemplo elucidador mas não exatamente análogo seria o que se obtém quando considera-se um baralho. Imposta a restrição de que todas as suas 54 cartas estejam em uma dada ordem pré-estabelecida, há apenas uma possibilidade de sequência para as cartas, ou seja, há apenas um microestado acessível a este sistema. Sua entropia seria, portanto, zero (pois ln 1 = 0). O número de microestados sobe para 54 se permitir-se que apenas uma dada carta esteja fora da ordem, e é significativamente maior se considerada a restrição de que apenas a primeira carta na sequência seja um ás. Se a restrição for relaxada ainda mais, impondo-se apenas que as cartas sejam as cartas de um único baralho completo (restrição antes também subentendida) o sistema terá o maior número de configurações possíveis, a maior desordem possível, e portanto a maior entropia possível. Aumentar a desordem, ou seja, a entropia de um sistema termodinâmico significa, de forma similar, dar-lhe condições para que haja um maior número de microestados acessíveis às partículas que o compõem.
A comparação com o baralho não é direta pois em sistemas termodinâmicos há de se considerar a indistinguibilidade das partículas (o que não ocorre com as cartas) e o que vem a ser um microestado, ou seja, uma configuração do sistema, entre outros pormenores, mas de forma geral, assim como ocorre para o baralho, a remoção de restrições impostas ao sistema em equilíbrio leva a um aumento na sua entropia. Importante também é observar que um aumento da energia interna U mantidas as restrições espaciais leva a um aumento de microestados acessíveis às partículas do sistema pois estas têm, agora, mais energia, e portanto a um aumento na entropia deste. A entropia cresce com a energia interna U de forma monótona para sistemas estáveis, o que significa dizer, em acordo com a definição de temperatura [Nota 3] absoluta, que, para sistemas em equilíbrio, a temperatura absoluta nunca pode ser negativa.
Há em verdade várias interpretações cientificamente corretas para o termo "desordem", e citar-se-á também uma oriunda da termodinâmica e diretamente associada à segunda lei da termodinâmica e ao estudo da máquina térmica e das transformações de energia (calor e trabalho) nestas máquinas. A segunda lei obriga que uma máquina térmica (ou um refrigerador) tenha necessariamente uma fonte quente e uma fonte fria. Um aumento da entropia representa, em tais sistemas, uma medida da energia que, oriunda da fonte quente, poderia ter sido aproveitada na forma de trabalho, mas, não o sendo, foi simplesmente "desperdiçada" como calor na fonte fria, tornado-se doravante indisponível para produzir o citado trabalho. A associação com desordem provém da observação de que trabalho em física envolve necessariamente variação de volume de uma parte do sistema, ou seja, o movimento direcionado de uma fronteira restritiva interna ao sistema isolado (a fronteira comum entre dois de seus subsistemas), e por conseguinte movimento direcionado, ordenado, de todas as partículas do subsistema delimitado por esta fronteira em movimento. Trabalho tem assim a ver com transferência de energia cinética (energia térmica), mas as partículas responsáveis por esta transferência movem-se de forma ordenada, direcionada, "acompanhando" a fronteira em movimento. Já a energia térmica trocada na forma de calor implica também variação da energia de movimento das partículas dos subsistemas, mas estas partículas agora movem-se de forma completamente desordenadas durante esta troca. O calor, oposto ao trabalho, implica a "propagação" de energia térmica mediante movimentos aleatórios - transferência de energia térmica (cinética) em forma não espacialmente direcionada -, feito de forma que a fronteira do sistema efetivamente não se move (o calor "passa" pela fronteira). Assim, o aumento de entropia, e portanto da desordem, de um sistema significa transformar parte do "movimento ordenado" das partículas de um sistema - que poderia ser usado para fazer trabalho - em movimento "desordenado", não associado a trabalho. O calor é a forma mais evidente de se fazer a entropia do sistema variar, ao passo que a troca de energia mediante trabalho por si só não implica variação da entropia, conforme visto.
Aumentar a desordem significa, assim, desperdiçar energia que poderia em princípio ser aproveitada como trabalho e, não o sendo, foi simplesmente entregue na forma de calor à fonte fria do sistema. Uma vez entregue à fonte fria, a energia atrelada ao aumento de entropia não pode mais, em contexto global, ser convertida em trabalho.
Entropia[editar | editar código-fonte]
Transformações reversíveis[editar | editar código-fonte]
A ideia de entropia, uma grandeza física que encontra sua definição dentro da área da termodinâmica [Nota 4] , surgiu no seguimento de uma função criada porClausius a partir de um processo cíclico reversível. Sendo Q o calor trocado entre o sistema e sua vizinhança e T a temperatura absoluta do sistema, em todo processo reversível a integral de curva de 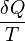 só depende dos estados inicial e final, sendo independente do caminho seguido. Portanto deve existir uma função de estado do sistema, S = f (P, V, T), chamada de entropia, cuja variação em um processo reversível entre os estados inicial e final é: [Nota 5]
só depende dos estados inicial e final, sendo independente do caminho seguido. Portanto deve existir uma função de estado do sistema, S = f (P, V, T), chamada de entropia, cuja variação em um processo reversível entre os estados inicial e final é: [Nota 5]
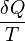 só depende dos estados inicial e final, sendo independente do caminho seguido. Portanto deve existir uma função de estado do sistema, S = f (P, V, T), chamada de entropia, cuja variação em um processo reversível entre os estados inicial e final é: [Nota 5]
só depende dos estados inicial e final, sendo independente do caminho seguido. Portanto deve existir uma função de estado do sistema, S = f (P, V, T), chamada de entropia, cuja variação em um processo reversível entre os estados inicial e final é: [Nota 5]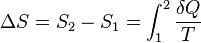 , sendo Q reversível
, sendo Q reversível
A entropia física, em sua forma clássica é dada por:
 , desde que o calor seja trocado de forma reversível
, desde que o calor seja trocado de forma reversível
ou, quando o processo é isotérmico:
O significado desta equação pode ser descrito, em linguagem corrente, da seguinte forma:
- Em processos reversíveis como o descrito, quando um sistema termodinâmico passa do estado 1 ao estado 2, a variação em sua entropia é igual à variação da quantidade de calor trocada (de forma reversível) dividido pela temperatura.
Processos de não equilíbrio[editar | editar código-fonte]
Em processos mais complexos, o que inclui os processos irreversíveis e de não equilíbrio como a expansão livre, entropia pode e sempre é produzida dentro do próprio sistema, e a variação total na entropia destes sistemas é igual à soma de dois termos: a entropia produzida e a entropia trocada com a vizinhança. A entropia trocada equivale, em processos quase estáticos, conforme descrito, à integral de dQ/T, sendo sempre nula quando a transformação é adiabática. O uso desta expressão ao casos de processos de não equilíbrio é contudo inadequado, ou, no mínimo, requer muita cautela, visto que a própria definição detemperatura fica comprometida. Já a entropia produzida vale zero apenas quando o processo é reversível, sendo sempre positiva em transformações irreversíveis.
Observa-se que em todas os processos a entropia total do sistema mais vizinhança ou aumenta (processos irreversíveis), ou fica constante (transformações reversíveis). Na prática, apesar de existirem processos que muito se aproximam dos reversíveis, toda transformação leva a um aumento na entropia total do sistema mais vizinhança, e este princípio permite definir a Segunda Lei da Termodinâmica, cuja implicação direta consiste no fato de que um processo tende a dar-se de forma espontânea em único sentido, aquele que leve ao aumento da entropia total (do sistema mais vizinhança). Por esses motivos, a entropia também é chamada de flecha do tempo.
Como não é possível determinar-se o aumento da entropia partindo-se diretamente de considerações sobre os sistemas que estão em processos de não equilíbrio - irreversíveis - justamente por estes estarem fora do equilíbrio, para determinar-se a variação de entropia total sofrida por um sistema ao longo de um processo de não equilíbrio determina-se a diferença entre as entropias inicial e final associadas aos respectivos estados de equilíbrio inicial e final. Tal consideração leva em conta o fato de a entropia ser uma função de estado, e por tal sua variação não depende de como o sistema saiu de um estado e chegou ao outro, e sim apenas dos estados inicial e final envolvidos.
A unidade de entropia no SI é designada por J/K'.
Definição termodinâmica[editar | editar código-fonte]
No início da década de 1850, Rudolf Clausius descreveu o conceito de energia desperdiçada em termos de diferenciais.
Em 1876, o físico, químico e matemático Willard Gibbs chegou à conclusão de que o conceito de energia disponível ΔG em um sistema termodinâmico é matematicamente obtido através da subtração entre aenergia perdida TΔS e a variação da energia total do sistema ΔH.
- - "Existe uma função (denominada entropia S) dos parâmetros extensivos de um sistema definida para todos os estados de equilíbrio termodinâmico deste sistema e com a seguinte propriedade: dentre todos os estados de equilíbrio possíveis que satisfazem as restrições físicas impostas ao sistema o estado de equilíbrio assumido pelo sistema será aquele para o qual os valores dos parâmetros extensivos neste estado levem à maximização do valor de sua entropia S. Em um sistema sem restrições internas a entropia é a maior possível."
A exemplo, na parte superior da figura ao lado tem-se um sistema com uma fronteira adiabática e uma restrição interna. O estado de equilíbrio termodinâmico de um sistema, satisfeitas as restrições internas, corresponde ao estado onde a entropia é a máxima possível. Na parte inferior a restrição é removida. O sistema passa por transformações e, após certo tempo atinge um novo estado de equilíbrio termodinâmico. Nestas transformações a entropia do sistema geralmente aumenta, o que ocorre para expansão livre mostrada, ou em casos outrem específicos - quando todos os processos se fazem de forma reversível - não se altera. A entropia de um sistema isolado nunca diminui.
Assim, o estado de equilíbrio realmente assumido por um sistema termodinâmico é, satisfeitas as restrições físicas impostas, o estado de maior entropia possível, e a remoção de uma restrição leva geralmente a um aumento da entropia do sistema composto, ou, em caso específicos (transformações reversíveis), à manutenção de seu valor, mas nunca a uma diminuição da mesma.
Há três outros postulados que, em termodinâmica, mostram-se diretamente associados à definição de entropia, sendo eles:
- - "A entropia de um sistema composto é aditiva sobre os subsistemas que o constituem. A entropia é contínua e diferenciável e é uma função monótona crescente da energia interna U."
- - "A entropia de um sistema é nula para um estado onde a temperatura absoluta T também o seja."
- - "Existe um estado particular - chamado estado de equilíbrio - de um sistema que, macroscopicamente, é completamente caracterizado pela energia interna U, pelo volume V, e pela quantidade de matéria N1, N2,N3 de seus constituintes químicos." [Nota 7] .
A entropia S quando expressa em função do volume V do sistema, da quantidade de partículas N do sistema e da energia interna U do sistema, S(U,N,V), é uma Equação Termodinâmica Fundamental para um sistema termodinâmico simples, e pode, mediante a Transformada de Legendre, ser transformada em outras equações fundamentais como a equação da Entalpia H(S,P,N), Energia de Helmholtz F(T,V,N), Energia livre de Gibbs G(T,P,N) ou o Grande Potencial Canônico U(T,P,m). Em sistemas termodinâmicos mais complexos, a exemplo em sistemas magnéticos, outras variáveis podem vir a figurar na equação entrópica fundamental e nas outras equações fundamentais, entretanto os conceitos de equação fundamental e transformada de Legendre permanecem os mesmos.
As equações fundamentais diferem das equações de estado basicamente no fato de que a partir de uma equação fundamental pode-se obter, com o uso do formalismo termodinâmico, qualquer informação a respeito do sistema termodinâmico por ela descrito, inclusive as equações de estado para este sistema, ao passo que o mesmo não pode ser feito a partir de uma equação de estado, que não retém em si todas as informações necessárias a respeito do sistema. É necessário um conjunto de equações de estado para a descrição completa de um sistema termodinâmico (do qual poderia obter-se, então, as equações fundamentais).
A Primeira Lei da Termodinâmica[editar | editar código-fonte]
A primeira lei da termodinâmica é a lei de conservação de energia aplicada aos processos térmicos. Nela observamos a equivalência entre trabalho e calor. Este princípio pode ser enunciado a partir do conceito de energia interna. Esta pode ser entendida como a energia associada aos átomos e moléculas em seus movimentos e interações internas ao sistema. Num sistema isolado a energia total permanece constante [Nota 8].
A Segunda Lei da Termodinâmica[editar | editar código-fonte]
A Segunda Lei da Termodinâmica, uma importante lei física, determina que a entropia total de um sistema termodinâmico isolado tende a aumentar com o tempo, aproximando-se de um valor máximo à medida que restrições internas ao sistema são removidas. O estado de equilíbrio termodinâmico de um sistema isolado corresponde ao estado onde, satisfeitas as restrições internas, a entropia é máxima. Duas importantes consequências disso são que o calor não pode passar naturalmente de um corpo frio a um corpo quente, e que um Moto perpétuo, ou seja, um motor que produza trabalho infinitamente, mas por calor, seja impossível [Nota 9] .
Interpretação estatística[editar | editar código-fonte]
Em 1877, Ludwig Boltzmann visualizou um método probabilístico para medir a entropia de um determinado número de partículas de um gás ideal, na qual ele definiu entropia como proporcional ao logaritmo neperiano do número de microestados que um gás pode ocupar:
Onde S é a entropia, k é a constante de Boltzmann e Ω é o número de microestados possíveis para o sistema.
O trabalho de Boltzmann consistiu em encontrar uma forma de obter a equação entrópica fundamental S a partir de um tratamento matemático-probabilístico [Nota 10] facilmente aplicável aos sistemas em questão. Ao fazê-lo, conectou o todo poderoso formalismo termodinâmico associado à equação fundamental a um método de tratamento probabilístico simples que exige apenas considerações físicas primárias sobre o sistema em análise, obtendo, a partir de considerações básicas, todo o comportamento termodinâmico do sistema. A equação de Boltzman mostra-se muito importante para o estudo termodinâmico de tais sistemas, e reconhecida como tal pelo próprio autor, encontra-se gravada em sua lápide [Nota 11] .
Superfícies isentrópicas[editar | editar código-fonte]
Superfícies isentrópicas são superfícies formadas por todos os pontos que apresentem, em um diagrama de estados - onde os eixos coordenados estão associados às grandezas termodinâmicas como pressão,volume e temperatura (etc.), e cada ponto representa um possível estado de equilíbrio termodinâmico do sistema -, o mesmo valor para a entropia S.
Transformações sofridas pelo sistema são expressas como linhas unindo uma sequência de pontos no diagrama de estados, ou como "saltos" entre estes pontos.
Para um sistema isolado que sofra apenas transformações reversíveis, as linhas que representam as mudanças de estado estão restritas à superfície isentrópica à qual pertence o estado inicial. O sistema pode ser levado de um estado inicial a qualquer outro estado representado por ponto sobre a mesma isentópica sem comprometer a possibilidade de retorno ao estado inicial, feita também sobre a mesma superfície isentrópica.
Transformações irreversíveis em sistemas isolados (como a expansão livre) conectam pontos em isentrópicas distintas. Uma vez descrito por ponto em outra isentrópica (de valor S maior), o sistema isolado jamais poderá retornar ao estado inicial, ficando todos os estados associados à isentrópica anterior inacessíveis ao sistema isolado, que agora pode assumir apenas configurações descritas por pontos na sua nova isentrópica, ou em isentrópicas superiores (com maiores valores de S).
O retorno do sistema a isentrópicas com menores valores de S só é possível mediante a troca de calor e de entropia com a vizinhança, e assim, neste caso, o sistema não poderá mais estar adiabaticamenteisolado. Tem-se então, em acordo com a Segunda Lei da Termodinâmica, uma redução na entropia do sistema às custas de um aumento na entropia global do conjunto sistema mais vizinhança.
Escoamentos isentrópicos são uma boa aproximação para os escoamentos atmosféricos reais em escala sinótica, nas regiões sem precipitação (por exemplo, nos escoamentos anticiclônicos, anti-horários noHemisfério Sul e horários no Hemisfério Norte) e em equilíbrio radiativo (o ganho é igual à perda da densidade de fluxo radiativo).
Ver também[editar | editar código-fonte]
- Termodinâmica
- Lei zero da termodinâmica
- Primeira lei da termodinâmica
- Segunda lei da termodinâmica
- Transformada de Legendre
- Entalpia
Notas
- ↑ A associação entre entropia e o conceito de "desordem" que vigora em "senso comum" (o de "bagunça") é possível, mas diga-se de passagem, por ser geralmente feita de forma muito pouco cautelosa, bem "delicada"!
- ↑ Em particular, a lei do "aumento da desordem", vale lembrar explicitamente - válida em sistemas isolados - não contraria outras teorias científicas como a teoria do Big Bang ou mesmo a teoria da evolução biológica, e quem as usa para "invalidar" tais teorias incorre em erro científico crasso.
- ↑ A temperatura é definida, em termodinâmica, como a derivada parcial da energia interna em relação à entropia:
 . Se a entropia cresce com o aumento de energia interna, esta derivada é necessariamente positiva
. Se a entropia cresce com o aumento de energia interna, esta derivada é necessariamente positiva - ↑ Para uma introdução um pouco aprofundada sobre Termodinâmica e suas Leis, sobre o conceito de diagramas e equações de estado, sobre equações fundamentais e potenciais termodinâmicos, sobre entropia, sobre aplicações práticas e mais, consulte: Termodinâmica, Teoria Cinética e Termodinâmica Estatística (Sears; Salinger).
- ↑ Para um introdução ao conceito de entropia, sua associação com processos reversíveis, irreversíveis e com a Segunda Lei da Termodinâmica, consulte Física 1 (Halliday; Resnick; Krane), cap. 26 entre outros.
- ↑ Para maiores esclarecimentos sobre o postulado da entropia e sobre os a ele associados, sobre as equações fundamentais e sobre a transformada de Legendre, consulte Thermodynamics and an Introduction to Thermostatistics (Callen), cap. 1.
- ↑ Erro de citação: Tag
<ref>inválida; não foi fornecido texto para as refs chamadas - ↑ Para uma introdução à Primeira Lei da Termodinâmica, consulte Física 2 (Halliday, Resnick, Krane), cap. 25.
- ↑ Para uma introdução à Segunda Lei da Termodinâmica, consulte Física 2 (Halliday, Resnick, Krane), cap. 26.
- ↑ Para uma melhor compreensão do trabalho de Boltzmann no contexto da termodinâmica estatística e para uma introdução (matemática e elucidativa) ao estudo estatístico de sistemas termodinâmicos e ao formalismo termodinâmico associado às equações fundamentais, consulte: Introdução à Física Estatística (Salinas, R. A.).
- ↑ Uma foto do túmulo de Boltzmann em Viena, mostrando a equação S=k log w, pode ser encontrada no frontispício do livro Introdução à Física Estatística (Salinas, Sílvio R. A.)
<ref> definido em <references> não tem um atributo de nome.Referências
- ↑ Em acordo com Callen, Herbert B. - Thermodynamics and An Introduction to Thermostatics - John Wiley & Sons - ISBN 0-471-86256-8
Bibliografia[editar | editar código-fonte]
- Halliday, David; Resnick, Robert; Krane, Kenneth S.. Física (volumes 1,2, 3 e 4). Rio de Janeiro: LTD Livros Técnicos e Científicos Editora, 1996. ISBN 0
- Callen, Herbert B.. Thermodynamics and an Introduction to Thermostatics Second edition. Nova Iorque: John Wiley & Sons Inc., 1985. ISBN 0-471-86256-8
- Sears, Francis W; Salinger, Gerhard L.. Termodinâmica, Teoria Cinética, e Termodinâmica Estatística.. Rio de Janeiro: Guanabara Dois, 1979.
- Salinas, Sílvio R. A.. Introdução à Física Estatística. São Paulo: Editora da Universidade de São Paulo, 1999. ISBN 85-314-0386-3Em termodinâmica, entropia é a medida de desordem das partículas em um sistema físico. Utiliza-se a letraS para representar esta grandeza.Comparando este conceito ao cotidiano, podemos pensar que, uma pessoa ao iniciar uma atividade tem seus objetos organizados, e a medida que ela vai os utilizando e desenvolvendo suas atividades, seus objetos tendem a ficar cada vez mais desorganizados.Voltando ao contexto das partículas, como sabemos, ao sofrem mudança de temperatura, os corpos alteram o estado de agitação de suas moléculas. Então ao considerarmos esta agitação como a desordem do sistema, podemos concluir que:
- quando um sistema recebe calor Q>0, sua entropia aumenta;
- quando um sistema cede calor Q<0, sua entropia diminui;
- se o sistema não troca calor Q=0, sua entropia permanece constante.
Segundo Rudolf Clausius, que utilizou a idéia de entropia pela primeira vez em 1865, para o estudo da entropia como grandeza física é mais útil conhecer sua variação do que seu valor absoluto. Assim, Clausis definiu que a variação de entropia (ΔS) em um sistema como:Para processos onde as temperaturas absolutas (T) são constantes.Para o caso onde a temperatura absoluta se altera durante este processo, o cálculo da variação de entropia envolve cálculo integral, sendo que sua resolução é dada por:Observando a natureza como um sistema, podemos dizer que o Universo está constantemente recebendo energia, mas não tem capacidade de cedê-la, concluindo então que a entropia do Universo está aumentando com o passar do tempo.Entropia é um conceito da termodinâmica que mede a desordem das partículas de um sistema físico.A entropia é uma grandeza na termodinâmica, representada nas formulações da física pela letra S.De acordo com a Lei da Termodinâmica, quanto maior for a desordem de um sistema, maior será a sua entropia.Por exemplo, quando alguém entra na cozinha encontra todos os utensílios e ingredientes organizados, conforme vai cozinhando, as coisas começam a se desorganizar.Da mesma forma seria o sistema da entropia, ou seja, quanto maior o processo de alteração de um estado, maior será a sua desordem.As entropias são espontâneas, isso quer dizer que seguem princípios da natureza, não sendo irreversíveis.Por exemplo, quando um copo com água cai no chão, o resultado da bagunça gerada é a entropia deste ato, no entanto, seria impossível fazer a água voltar para o copo, sendo impossível retroceder a entropia.Etimologicamente, o termo entropia se originou a partir do grego entropêe, que significa “em mudança”.Entropia negativa
A entropia negativa, no âmbito da organização administrativa, é a definição dada a empresa, companhia ou sistema que está se restabelecendo, ou seja, se recuperando da desordem e falência.O conceito da entropia negativa consiste em reverter a entropia, o estágio de “bagunça” e “caos”.A entropia negativa também é chamada de “informação”, pois de acordo com o princípio da entropia, quanto maior a informação, menor a desordem.Entropia e Entalpia
Entalpia (representada pela letra “H”) é o nome atribuído à energia que fica armazenada nas substâncias (energia interna), a espera que sofra alguma transformação para que seja alterada ou liberada.Já a entropia é a grandeza que mede a energia que não é capaz de ser transformada em trabalho.Ver também o significado de energia.



 a quantidade de
a quantidade de 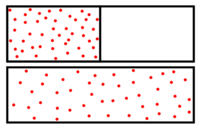
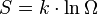
Nenhum comentário:
Postar um comentário