Combustão Parcial e Completa
Na indústria, as reações de combustão acontecem a todo o momento e possuem finalidades variadas: desde a geração de vapor para movimentar turbinas e equipamentos, até o fornecimento de energia para iniciar novas reações. E, como a oxidaçãocompleta dos combustíveis libera mais energia que a parcial, a mesma se faz mais desejável.
A diferença entre os produtos das duas oxidações (completa e parcial) está na presença do oxigênio nas moléculas: os produtos da combustão completa estão saturados com átomos de oxigênio, ao contrário dos produtos da combustão parcial que possuem a capacidade de absorver mais oxigênio se uma nova combustão lhes for promovida.
Exemplo: 20 mols de metano foram adicionados em um reator de combustão com quantidade suficiente de oxigênio. Em seguida, uma fonte de ignição iniciou a reação que possui 85% de eficiência na produção de dióxido de carbono. Pede-se para calcular a porcentagem molar dos gases de exaustão do reator.
Resolução:
Sejam as respectivas reações de oxidação completa e parcial do metano:
CH4 + 2O2 -> CO2 + 2H2O (85%)
CH4 + 1,5O2 -> CO + 2H2O (15%)
Como a oxidação do metano ocorre com 85% de eficiência, 17 mol se oxidarão completamente e 3 mol se oxidarão parcialmente. Assim, de acordo com a estequiometria da reação, serão formados: 17 mol de CO2, 3mol de CO e 40 mol de H2O (proveniente das duas oxidações).
A soma final do número de mols dos gases é: 17+3+40 = 60 mol , de onde:
Os processos de combustão são responsáveis pela produção de cerca de 85 % da energia do mundo, inclusive o Brasil, em transporte (carros, aviões, trens, navios, etc), usinas termoelétricas, processos industriais, aquecimento doméstico, geradores, cozimento de alimentos e outro. Em uma reação estequiométrica ideal de um hidrocarboneto em ar são formados apenas CO2 e H2O, sendo o N2 um gás inerte.
De uma forma geral: CxHyOzNt + (x+y/4-z/2)[O2 + 3,76N2] → xCO2 + (y/2)H2O + (y/2)H2O + [t/2+3,76(x+y/4-z/2)]N2.
CH4 + 2 O2 → CO2 + 2 H2O +calor
Índice
[esconder]Tipos de combustão[editar | editar código-fonte]
Lenta[editar | editar código-fonte]
Quando se produz a uma temperatura suficientemente baixa, isto é, inferior a 500 °C, não havendo, regra geral, emissão de luz. A oxidação de um metal (ferro, cobre, zinco, etc.) em contacto com o ar úmido é um exemplo deste tipo de combustão. A combustão lenta é uma forma de queima que acontece a baixas temperaturas. A respiração celular e formação de ferrugem são exemplos de combustões lentas.
Viva[editar | editar código-fonte]
É aquela em que se produz chama e, vulgarmente, designa-se por fogo. Neste caso, devido à mistura dos gases inflamados com o ar forma-se a chama. No caso dos sólidos, cuja combustão decorre à superfície, verifica-se a incandescência a partir da sua ignição e também através da formação de brasas. Estas surgem quando o combustível já não liberta gases suficientes para provocar chama. A combustão do carvão ilustra estes aspectos.
Explosiva[editar | editar código-fonte]
Combustão resultante da mistura de gases ou partículas finamente divididas com o ar numa percentagem bem determinada – mistura explosiva ou detonante – propagando-se a uma velocidade superior a 340 m/s. Neste caso, a mistura tem de ocupar todo o espaço onde está contida e, no momento da explosão, provoca uma elevação de temperatura ou de pressão ou de ambas, simultaneamente, sobre todo o espaço confinante. Usamos como combustível a gasolina,o etanol ou o diesel. Combustão é o processo de obtenção de energia.
Combustão completa[editar | editar código-fonte]
Em uma combustão completa, o reagente irá queimar no oxigênio, produzindo um número limitado de produtos e uma chama oxidante, azul. Quando um hidrocarboneto queima no oxigênio, a reação gerará apenas dióxido de carbono  e água. Quando elementos como carbono, nitrogênio, enxofre e ferro são queimados, o resultado será os óxidos mais comuns. Carbono irá gerar o dióxido de carbono. Nitrogênio irá gerar o dióxido de nitrogênio
e água. Quando elementos como carbono, nitrogênio, enxofre e ferro são queimados, o resultado será os óxidos mais comuns. Carbono irá gerar o dióxido de carbono. Nitrogênio irá gerar o dióxido de nitrogênio  . Enxofre irá gerar dióxido de enxofre
. Enxofre irá gerar dióxido de enxofre  . Ferro irá gerar óxido de ferro (III)
. Ferro irá gerar óxido de ferro (III)  . A combustão completa é naturalmente improvável de ocorrer, a menos que a reação ocorra em situações cuidadosamente controladas, como, por exemplo, em um laboratório.
. A combustão completa é naturalmente improvável de ocorrer, a menos que a reação ocorra em situações cuidadosamente controladas, como, por exemplo, em um laboratório.
 e água. Quando elementos como carbono, nitrogênio, enxofre e ferro são queimados, o resultado será os óxidos mais comuns. Carbono irá gerar o dióxido de carbono. Nitrogênio irá gerar o dióxido de nitrogênio
e água. Quando elementos como carbono, nitrogênio, enxofre e ferro são queimados, o resultado será os óxidos mais comuns. Carbono irá gerar o dióxido de carbono. Nitrogênio irá gerar o dióxido de nitrogênio  . Enxofre irá gerar dióxido de enxofre
. Enxofre irá gerar dióxido de enxofre  . Ferro irá gerar óxido de ferro (III)
. Ferro irá gerar óxido de ferro (III)  . A combustão completa é naturalmente improvável de ocorrer, a menos que a reação ocorra em situações cuidadosamente controladas, como, por exemplo, em um laboratório.
. A combustão completa é naturalmente improvável de ocorrer, a menos que a reação ocorra em situações cuidadosamente controladas, como, por exemplo, em um laboratório.Combustão turbulenta[editar | editar código-fonte]
A combustão turbulenta é caracterizada por fluxos turbulentos. É a mais usada na indústria (ex: turbinas de gás, motores a diesel, etc.), pois a turbulência ajuda o combustível a se misturar com o comburente.
Combustão incompleta[editar | editar código-fonte]
Na combustão incompleta não há o suprimento de oxigênio adequado para que ela ocorra de forma completa. O reagente irá queimar em oxigênio, mas poderá produzir inúmeros produtos. Quando umhidrocarboneto queima em oxigênio, a reação gerará dióxido de carbono, monóxido de carbono, água, e vários outros compostos como óxidos de nitrogênio, dependendo da composição do combustível. Também há liberação de átomos de carbono, sob a forma de fuligem. A combustão incompleta é muito mais comum que a completa e produz um grande número de subprodutos. No caso de queima de combustível emautomóveis, esses subprodutos podem ser muito prejudiciais à saúde, ao meio ambiente e ao próprio carro.
Equação química[editar | editar código-fonte]
Geralmente, a equação química para queimar um hidrocarboneto (como o octano) com oxigênio é a seguinte:
- CxHy + (x + (y/4))O2 → xCO2 + (y/2)H2O
Por exemplo, a queima de propano é:
- C3H8 + 5O2 → 3CO2 + 4H2O
A equação, em síntese, de uma hidrocarboneto é sempre a seguinte:
- Combustível + Oxigênio → Dióxido de carbono + Água + Calor
A combustão é uma reação de uma substância (combustível) com o oxigênio  (comburente) presente na atmosfera, com liberação de energia.
(comburente) presente na atmosfera, com liberação de energia.
 (comburente) presente na atmosfera, com liberação de energia.
(comburente) presente na atmosfera, com liberação de energia.
A liberação ou consumo de energia durante uma reação é conhecida como variação da entalpia (ΔH), isto é, a quantidade de energia dos produtos da reação (Hp) menos a quantidade de energia dos reagentes da reação (Hr):
ΔH = Hp - Hr
Quando ΔH > 0 isto significa que a energia do(s) produto(s) é maior que a energia do(s) reagentes(s) e a reação é endotérmica, ou seja, absorve calor do meio ambiente. Quando ΔH < 0, isto significa que a energia do(s) reagente(s) é maior que a energia do(s) produto(s) e a reação é exotérmica, ou seja, libera calor para o meio ambiente, como no caso da combustão da gasolina, por exemplo.
A respiração é um processo de combustão (“queima de alimentos”) que libera energia necessária para as atividades realizadas pelos organismos. É interessante notar que a reação inversa da respiração é a fotossíntese, que ocorre no cloroplasto das células vegetais, onde são necessários gás carbônico, água e energia (vinda da luz solar) para liberar oxigênio e produzir material orgânico (celulose, glicose, amido, etc.) utilizado no crescimento do vegetal.
combustão/respiração[editar | editar código-fonte]
C6H12O6(s) + 6 O2(g) ↔ 6 CO2(g) + 6 H2O (l) + energia
Fotossíntese[editar | editar código-fonte]
A gasolina possui enxofre (S), e o diesel, ainda mais. Hoje no Brasil existe um grande investimento por parte da Petrobras para diminuir a concentração de enxofre no diesel e assim torná-lo menos poluente. Portanto, combustíveis que tem enxofre, ao serem queimados produzem grandes quantidades de um gás bastante tóxico e corrosivo, responsável por acidificar a atmosfera, o dióxido de enxofre (SO2). Já o álcool é um combustível que não apresenta enxofre e portanto não produz o dióxido de enxofre.
S(s)+ O2(g ) → SO2(g)
A falta de oxigênio durante a combustão leva à chamada ‘combustão incompleta’ que produz monóxido de carbono (CO). Note que o CO tem um oxigênio a menos que o CO2, o que caracteriza a deficiência de oxigênio, ou a ineficiência da reação. Este gás é muito tóxico para o ser humano, pois este dificulta a função da hemoglobina, que é responsável pela renovação do oxigênio no nosso sangue. Pequenas concentrações de monóxido de carbono já provocam tonturas e dores de cabeça. Outro produto indesejável da combustão incompleta é a fuligem (C), que não tem oxigênio na sua constituição. A porção mais fina da fuligem pode impregnar nos pulmões e causar problemas respiratórios.
As equações químicas abaixo ilustram a quantidade de calor (ΔH) liberada durante a combustão completa e incompleta do gás metano (CH4). Note como a quantidade de calor liberado é menor nos casos de combustão incompleta. Portanto, além da combustão incompleta gerar compostos nocivos à saúde humana, há também uma grande desvantagem econômica, pois com a mesma quantidade de combustível haverá menor quantidade de energia gerada! Veja as equações:
Combustão completa do metano:
CH4(g) + 2O2(g) → CO2(g) + 2H2O (l) ΔH = - 802 kJ/mol (energia liberada)
Combustão incompleta do metano:
CH4(g) + 3/2 O2(g) → CO(g) + 2H2O(l) ΔH = - 520 kJ/mol
CH4(g) + O2(g) → C(s) + 2H2O(l) ΔH = - 408,5 kJ/mol
É muito importante saber a quantidade de calor liberada pelos combustíveis para que seja possível comparar o valor energético de cada um deles. Na Tabela 1 são mostradas as entalpias de combustão (ΔHo) para alguns combustíveis, isto é, a energia liberada na queima completa de um mol do combustível. O zero utilizado como índice superior indica que as condições iniciais dos reagentes e as finais dos produtos são 25o C e 1 atm, chamadas de condições padrão.
O combustível menos poluente que se conhece é o hidrogênio, pois sua combustão gera apenas água: H2(g) + ½ O2(g) → H2O(l) ΔH = - 286 kJ/mol
Combustão de combustíveis líquidos[editar | editar código-fonte]
A combustão de um combustível líquido em uma atmosfera oxidante acontece na verdade em forma gasosa. Isto quer dizer, quem queima é o vapor, não o líquido. Portanto, um líquido inflamável normalmente só irá pegar fogo acima de uma certa temperatura, que é seu ponto de fulgor. Abaixo dessa temperatura, o líquido não irá evaporar rápido o suficiente para sustentar o fogo caso a fonte de ignição seja removida.
Combustão de combustíveis sólidos[editar | editar código-fonte]
O ato da combustão consiste em três fases relativamente distintas, mas que se sobrepõem:
- Fase de pré-aquecimento, quando o combustível não queimado é esquentado até o seu ponto de fulgor e depois para seu ponto de combustão. Gases inflamáveis começam a ser envolvidos em um processo similar à destilação seca.
- Fase de destilação ou fase gasosa, quando a mistura dos gases inflamáveis com oxigênio sofre ignição, energia é produzida em forma de calor e luz. Fogo normalmente é visível nesta fase.
- Fase de carvão ou fase sólida, quando a saída de gases inflamáveis é muito pouca para a presença persistente de chama, e o combustível carbonizado queima lentamente. Ele só fica incandescente e depois continua a arder sem chama.
Temperaturas para a combustão[editar | editar código-fonte]
Assumindo condições de combustão perfeitas, como uma combustão adiabática(sem perda de calor) e completa, a temperatura da combustão pode ser determinada. A fórmula que leva a essa temperatura é baseada na primeira lei da termodinâmica e se aproveita do fato que o calor da combustão (calculado a partir do valor de aquecimento do combustível) é usado inteiramente para aquecer o combustível e o gás (ex: oxigênio ou ar)
No caso de combustíveis fósseis queimados no ar, a temperatura de combustão depende:
- do valor de aquecimento
- da proporção do ar em relação ao combustível (
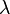 )
) - da capacidade térmica do combustível e do ar
- as temperaturas de entrada do ar e combustível
A temperatura de combustão adiabática aumenta para:
- valores de aquecimento mais altos
- temperaturas de entrada mais altas
- proporções entre o ar e o combustível tendendo para 1.
Normalmente, a temperatura de combustão adiabática para o carvão mineral é por volta de 1500 °C (para temperaturas de entrada e temperaturas do ambiente e  ), cerca de 2000 °C para o óleo e 2200 °C para o gás natural.
), cerca de 2000 °C para o óleo e 2200 °C para o gás natural.
 ), cerca de 2000 °C para o óleo e 2200 °C para o gás natural.
), cerca de 2000 °C para o óleo e 2200 °C para o gás natural.Análise por combustão[editar | editar código-fonte]
A análise da combustão é um processo usado para determinar a composição de um composto orgânico.
Ver também[editar | editar código-fonte]
- Fogo
- Combustão humana espontânea
- Teoria do flogisto
- Aquecimento globalO Fogo uma reação química de oxidação com desprendimento de luz e calor, esta reação é denominada de combustão. Para que isso ocorra é necessário a união de quatro elementos essenciais do fogo, que são:
- Combustível - É toda substancia capaz de de queimar e alimentar a combustão. Ele serve de campo de propagação ao fogo. Os combustíveis podem ser, sólidos, líquidos ou gasosos. Ex.: madeira, papel, tinta, algodão, álcool, gasolina, etc.
- Comburente - É o elemento que dá vida às chamas, e intensifica a combustão. O mais comum é que o oxigênio desempenhe este papel, porem não é o único, existindo outros gases.
- Calor - Forma de energia que eleva a temperatura. Gerada da transformação de outra energia, através de processo físico ou químico. É a condição favorável causadora da combustão.
- Reação em cadeia - É a queima auto-sustentável. É a união dos três itens acima descritos, gerando uma reação química. Quando o calor irradiado das chamas atinge o combustível e este é decomposto em partículas menores, que se combinam com o comburente e queimam, irradiando outra vez calor para o combustível, formando um ciclo constante.
A retirada de um ou mais dos componentes acima citados resulta em extinção da combustão.FORMAS DE COMBUSTÃO
- Combustão Completa: É aquela em que a queima produz calor e chamas e se processa em ambiente rico em comburente.
- Combustão Incompleta: É aquela em que a queima produz calor e pouca ou nenhuma chama e se processa em ambiente pobre em comburente.
- Combustão Espontânea: É aquela gerada de maneira natural, podendo ser pela ação de bactérias que fermentam materiais orgânicos, produzindo calor e liberando gases. Alguns materiais entram em combustão sem fonte externa de calor. Ocorre, também, na mistura de determinadas substâncias químicas, quando a combinação gera calor e libera gases.
- Explosão: É a queima de gases ou partículas sólidas em altíssima velocidade, em locais confinados.
FORMAS DE PROPAGAÇÃO
O calor pode-se propagar de três diferentes maneiras: Condução, Convecção e Irradiação. Como tudo na natureza tende ao equilíbrio, o calor é transferido de objeto com temperatura mais alta para aqueles com temperatura mais baixa. O mais frio de dois objetos absorverá calor até que esteja com a mesma quantidade de energia do outro.- Condução - É a transferência de calor através de um corpo sólido de molécula a molécula. Quando dois ou mais corpos estão em contato, o calor é conduzindo através deles como se fosse um só corpo.
- Convecção - É a transferência de calor pelo próprio movimento ascendente de massas de gases ou líquido.
- Irradiação - É a transmissão de calor por ondas de energia caloríficas que se deslocam através do espaço.As reações de combustão estão presentes em muitos aspectos do nosso cotidiano. Por exemplo, as principais fontes de geração de energia resultam da combustão ou queima de determinados combustíveis, como o etanol, a gasolina, o carvão vegetal, entre outros. Além disso, a energia da qual necessitamos para sobreviver e para realizar trabalho é resultado de reações de combustão que ocorrem dentro de nossas células, quando “queimamos” a comida ingerida.Mas o que é necessário para que haja uma reação de combustão?São necessárias três coisas:Esses três fatores compõem o triângulo de fogo, pois depois que se dá início à reação de combustão, a energia liberada sustenta a reação e permite que ela continue até que o combustível, o comburente ou o calor (energia liberada), acabe. Isso significa que ocorrerá uma reação em cadeia.Por exemplo, se alguém jogar um cigarro aceso em uma floresta, haverá uma queimada (reação de combustão). Nesse caso, o mato é o combustível, ooxigênio presente no ar atmosférico é o comburente e o cigarro aceso foi a fonte de ignição. Essa queimada irá continuar até que um dos três fatores seja eliminado. Se os bombeiros jogarem água, o calor será eliminado. Mas mesmo que nada seja feito para interromper essa queimada, ela acabará em algum momento, isto é, quando o combustível (mato) acabar.Conforme já mencionado, nessas reações há liberação de calor, assim, a combustão é uma reação exotérmica. No entanto, esse tipo de reação é uma combustão incompleta. Para entender o porquê, veja a diferença entre a combustão completa e a incompleta:Combustão completa:Analisando compostos orgânicos como combustíveis, temos que:
A combustão completa ocorrerá quando for feita a ruptura da cadeia carbônica e a oxidação total de todos os átomos de carbono da cadeia carbônica. Os produtos formados por hidrocarbonetos serão o CO2(dióxido de carbono) e H2O (água). Observe a combustão completa do isoctano, que é um dos componentes da gasolina.C8H18(g) + 25/2 O2 (g) → 8 CO2(g) + 9 H2O(l)Combustão incompletaNesse caso, não há quantidade de comburente, ou seja, de oxigênio suficiente para queimar todo o combustível. Assim, os produtos formados são CO (monóxido de carbono) e H2O. Observe a mesma combustão do isoctano, no entanto, agora de modo incompleto:C8H18(g) + 17/2 O2 (g) → 8 CO (g) + 9 H2O(l)A queimada das florestas é um exemplo, pois as emissões resultantes constituem-se em CO e matéria particular, como a fuligem (C), além de cinzas e outros compostos orgânicos simples e complexos. Pode-se formar também óxido de nitrogênio, ozônio e aldeídos, em virtude de reações secundárias pela presença de outros componentes do ar.C8H18(g) + 9/2 O2 (g) → 8 C (g) + 9 H2O(l)
Por Jennifer Fogaça
Graduada em Química
Equipe Brasil Escola
Nenhum comentário:
Postar um comentário